前回の記事では、身体組成分析技術の進化について見てきました。水中体重測定から精密な中性子放射化分析まで、それぞれ異なる方式で身体の秘密を解読しようと試みてきました。これらの技術が発展する一方で、もう一つの探索の道筋も静かに芽生えていました。この道筋が依拠していたのは、すでに存在していながら長期間見過ごされていた現象でした。それでは、生体電気インピーダンス分析が基礎的な電気学研究からどのように現代医学における重要な診断ツールへと発展したのかを見ていきましょう。
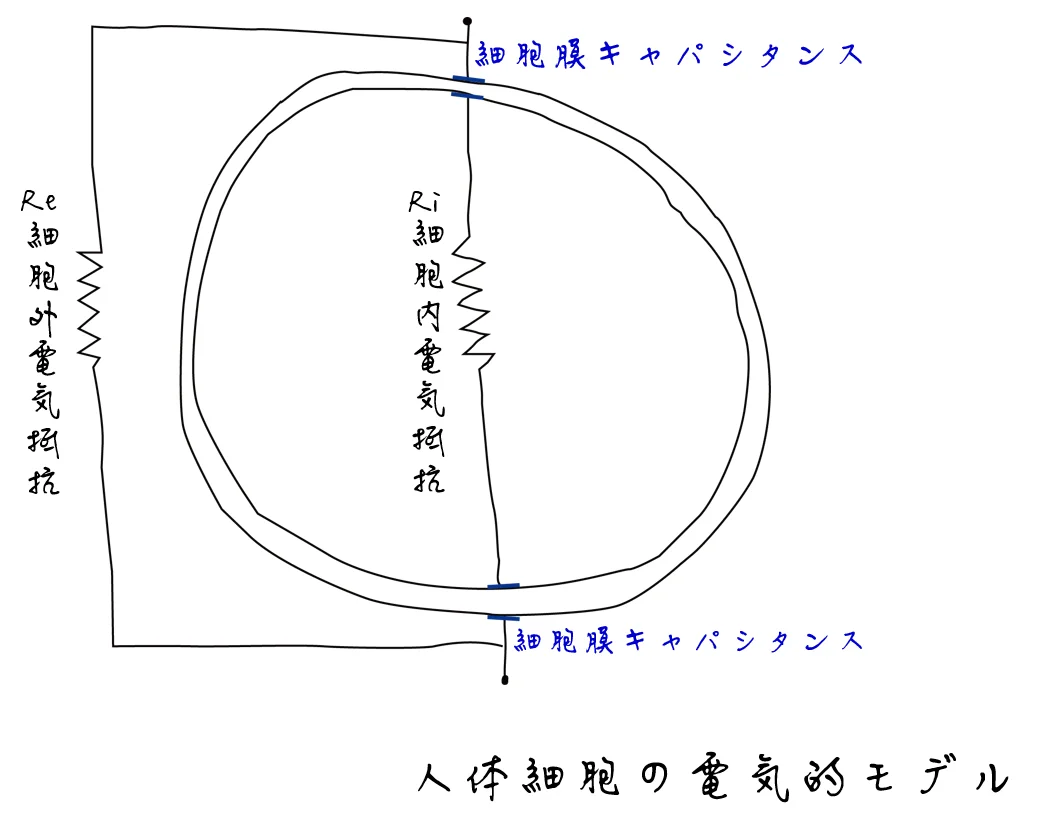
生体電気インピーダンス分析(Bioelectrical Impedance Analysis, BIA)の概念は、最も早くは1871年に遡ります。[1]当時の科学者たちは生体組織にも電気的特性があることを初めて発見し。1925年から1936年にかけて、研究者たちは等価回路モデルを確立して、後の発展の基礎を築きました。
隠された心臓の声
1940年代、医師たちはある難題に直面していました。開胸せずに心臓の機能を理解するにはどうすればよいのか、という問題です。聴診器は心拍の音を教えてくれますが、心臓が実際にどれだけの血液を送り出しているのか、血管内の血流がどのように変化しているのかといった重要な情報は身体の深部に隠されており、知る術がありませんでした。
そこで、科学者のニボアらは大胆な試みに着手しました。彼らは血液の導電性が他の組織よりもはるかに優れていることに注目し、微小な電流を身体に通せば、おそらく電気抵抗の変化から血流の変化を見出すことができるのではないかと推測しました。[2]
このアイデアから生み出されたのがインピーダンス血管造影術です。医師たちは腕や脚に電極を貼り付け、心臓が収縮すると血液が動脈に流れ込み、電気抵抗が低下し、心臓が拡張すると血流が減速し、電気抵抗が再び上昇したことを確認しました。このようにして、彼らは初めて血管内の血液の流動リズムを「見る」ことができたのです。
その後まもなく、クビチェックらはさらに一歩進んで、この概念を胸腔に応用し、心臓が収縮するたびに胸腔内の血液分布の変化が電気抵抗測定に反映されることを発見しました。精密な計算を通じて、心臓が1回の拍動で送り出す血液量を推定することにも成功したのです。この胸部生体電気インピーダンス技術により、医師たちは初めて非侵襲的に心機能を監視するツールを手に入れました。
視野の拡大
1960年代になると、科学者たちは別の問題について考え始めました。すなわち、同じ電気的原理を利用して身体全体の組成を理解できるのでは?ということです。そもそも、筋肉、脂肪、骨の含水量はすべて異なるわけで、それらの導電性も自然と差異が存在しているはずです。
1962年、トマセットは初めて多周波BIAを使用して人体の総水分量と細胞外水分を予測することを提案し、この分野に新たな可能性を開拓しました。真の突破口が訪れたのは1969年のこと。研究者のホッファーらがある実験を行い、健康な人と患者の全身電気抵抗を測定しながら、同時に他の方法で体内総水分量を測定したのです。彼らは身長の二乗を電気抵抗値で割った値(身長²/電気抵抗)が体内総水分量と高い相関を示すことを発見し、統計的相関係数は0.92から0.93に達しました。これをもとに、電気抵抗測定を通じて体内水分含有量を正確に予測できるようになり、身体の奥義が数値の対応関係の中で徐々に明らかになったのです。
この発見により、BIAの臨床応用の扉が開かれました。1985年、ルカスキらはさらに単一周波数BIAを発展させ、50kHzの周波数を使用して除脂肪組織の重量を評価しました。これ以降、栄養士や医師たちは簡単なツールを手に入れ、手足に電極を貼り付けるだけで身体組成を迅速に理解できるようになりました。
理想と現実のギャップ
物語はここで終わりません。研究者たちはすぐに、単一周波数には限界があることを発見しました。低周波電流は主に細胞外液を通過し、高周波電流は細胞膜を透過して細胞内部に入ることができます。そこで、多周波生体電気インピーダンススペクトル分析(BIS)が生まれました。4から1000kHzの広帯域範囲を通じて、理論的には細胞内外の水分を別々に測定できるようになったのです。

しかし、現実は往々にして理論よりも複雑です。これらの技術を実際の患者に適用したとき、研究者たちはその精度が大幅に低下することを発見しました。肥満患者、腎臓病患者、心不全患者の測定結果は、しばしば予想結果と大きく乖離していました。
実は、これらの予測式は過度に理想化された仮定の上に構築されていました。人体を標準的な円筒形導体として扱い、水分が体内に均一に分布し、各部位の組織組成が互いに類似していると仮定していましたが、実際の身体はそうではありません。すべての人間の腕、胴体、脚は、それぞれ独自の形状を持ち、筋肉と脂肪の分布も人によって異なります。疾患が現れると、これらの個体の独自性はさらに顕著になります。心不全は下肢浮腫を引き起こす可能性があり、腎臓疾患は全身の水分バランスに影響します。これらの変化により、予測式の誤差はさらに大きくなりました。
シンプル思考への回帰
予測モデルの困難に直面して、1990年代の研究者たちは改めて再考し始めました。もしかして、私たちは問題を複雑に考えすぎていたのではないか?そこで、イタリアのピッコリらがある提案を投げかけました。今となっては意外なほどシンプルな考え方ですが、複雑な予測式に頼るので、なぜ電気抵抗とリアクタンスの生の数値を直接使用しないのか?ということでした。
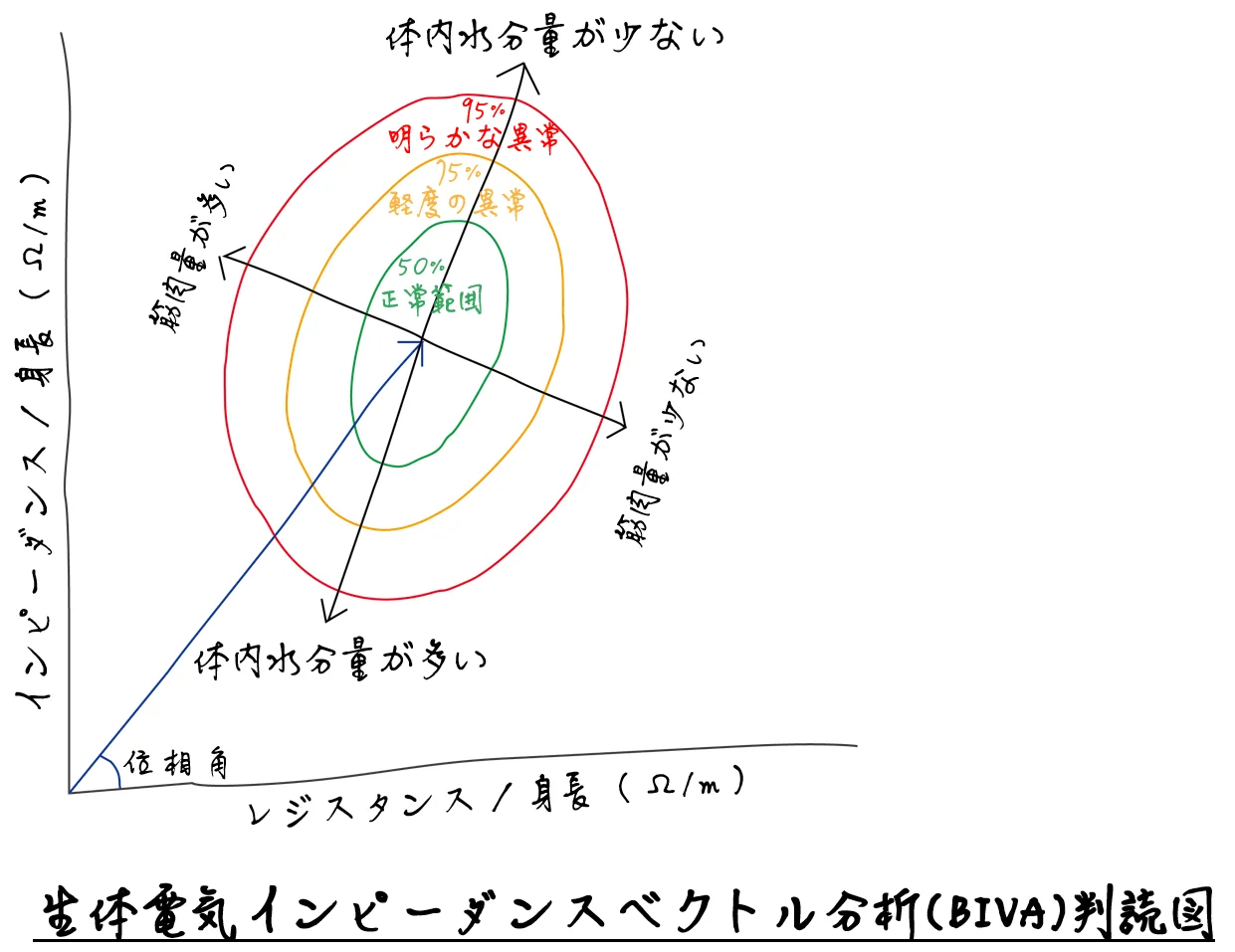
このアイデアから生まれたのが生体電気インピーダンスベクトル分析(BIVA)です。彼らは電気抵抗とリアクタンスをベクトル図として描き、健康な集団のベクトル分布が規則的な楕円形パターンを示すことを発見しました。それぞれの生理状態によって図上における位置は異なります。脱水や浮腫状態は水分軸方向の位置を牽引し、筋肉量の増減はもう一方の軸方向の分布を左右します。この図を通じて、医師は患者の水分状態と身体組成を同時に読み取ることができるようになりました。
位相角の啓示
これを基礎として、研究者たちは位相角という一見シンプルなパラメータが、実は身体に関する多くの秘密を秘めていることを発見しました。位相角は細胞膜の完全性、そして細胞の活力状態さえも反映していたのです。健康な細胞膜は安定したキャパシタンス機能を維持することができ、より大きな位相角を生み出します。一方、損傷した細胞や老化した細胞では位相角が低下します。
この発見により、BIAの臨床における新たな可能性が開拓されました。研究者たちは、がん患者の位相角が5度未満の場合、通常予後が悪く、位相角が1度増加するごとに患者の生存率が25%向上する可能性があることを発見しました。一見シンプルな数値が、医師に患者の将来についてこれほどまでに多くの情報を伝えることができるのです。
また、この技術は、より精密な局所測定へと発展していきました。乳がん術後のリンパ浮腫患者に対して、医師たちは患肢と健肢のインピーダンスの差を比較し始め、まだ明らかな腫脹が現れていない早期のリンパ浮腫でさえ、早期発見ができるようになりました。創傷治癒の過程において、研究者たちは電気抵抗の上昇が組織の修復を意味し、低下は感染や他の問題を示唆している可能性があることを発見しました。
この技術発展の軌跡は、さながら継続的に理解を深化させるプロセスのようです。最初の心血管モニタリングから、身体組成分析への試み、そして複雑な現実に直面した際の再考、最終的には基本的な電気パラメータに対するより深い認識への回帰。それぞれの転換点が、この技術をより実用的かつ信頼性の高いものにしてきました。
BIAの現在と未来
BIA技術は、生理機能モニタリングから身体組成分析、そして臨床応用へと回帰する「迂回の旅」を歩んできました。現代の発展は、位相角やBIVAといった生の電気パラメータの使用へと傾倒しており、複雑な予測モデルに依存することはなくなっています。このような原点回帰が、むしろより正確で実用的な臨床情報を提供しています。
継続的に技術が進歩する中、BIAは個別化医療における重要な監視ツールとなることが期待されています。この一見シンプルな電気測定技術は、現代医学に新たな窓を開いているのです。
注:BIA技術は便利ではあるものの、特殊な状況下における測定結果は依然として専門医療従事者の解釈が不可欠となります。健康面での懸念がある場合は、専門の医療従事者にご相談ください。
参考文献:
[1]Kyle, U. G., Bosaeus, I., De Lorenzo, A. D., et al. (2004). Bioelectrical impedance analysis—part I: review of principles and methods. Clinical Nutrition, 23(5), 1226-1243.
[2]Lukaski, H. C. (2013). Evolution of bioimpedance: a circuitous journey from estimation of physiological function to assessment of body composition and a return to clinical research. European Journal of Clinical Nutrition, 67, S2-S9.